Omega-3家族的长链多不饱和脂肪酸(n-3 PUFAs),也就是我们现在所熟知的鱼油(主要成分是DHA和EPA),除了被报道可以降低心血管疾病风险,鱼油还被发现对糖尿病、癌症、阿尔兹海默症在内的多种疾病具有益处。另一方面,大量的临床试验和流行病学调查则得出了很多相反的结论。鱼油对于人体的健康究竟有没有益处,直到现在依然存在很大的争议。这其中一个很重要的原因就在于n-3 PUFAs的作用机制一直没有被研究清楚。
2022年3月15日,复旦大学附属妇产科医院/代谢与整合生物学研究院赵世民教授、复旦大学生物医学研究院徐薇研究员、复旦大学生命科学学院赵健元研究员以及我组组长叶明亮研究员合作在Cell Reports上发表了题为Methylene-bridge tryptophan fatty acylation regulates PI3K-AKT signaling and glucose uptake的研究文章,报道多不饱和脂肪酸会修饰蛋白质色氨酸形成一种新的蛋白质酯化修饰,并揭示了DHA和EPA修饰激活PI3K-AKT信号和调控血糖吸收的分子机制(Cell reports 38 (11) , pp.110509;https://doi.org/10.1016/j.celrep.2022.110509)。
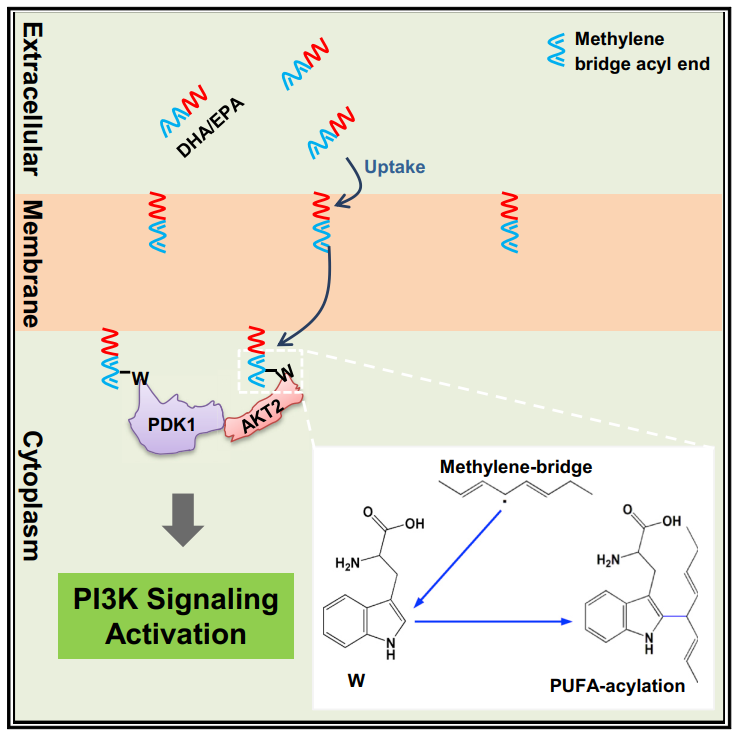
借助我组科研人员发展的Ti4+-IMAC磷酸化蛋白组学分析策略,研究人员发现胰岛素信号通路是受PUFA修饰调控的潜在信号通路,并且发现DHA和EPA会通过修饰该通路中的PDK1和AKT2蛋白来直接激活胰岛素通路:首先,外源添加的DHA和EPA会被细胞摄取并整合到细胞膜的磷脂中;接下来,细胞膜中 DHA 和 EPA 会由于磷脂的运动修饰到被PIP3招募至细胞膜附近的PDK1 和 AKT2上。最后,DHA和EPA修饰会促进PDK1和AKT2上膜并激活AKT下游信号。这一工作不仅揭示了一种全新的蛋白质酯化修饰,同时也为目前临床上观察到的n-3 PUFAs 复杂的生理现象提供了可能的机制解释。该工作被“BioArt”公众号进行了特别推送报道(https://mp.weixin.qq.com/s/OI_AELSKK8s9bfj7vL7MFQ)
Ti4+-IMAC是我国科学家首次建立并发展起来的、基于新机理的新一代固定金属离子亲和色谱材料,其磷酸肽富集特异性高达95%以上,富集效率比传统IMAC材料提高了3-5倍,比TiO2提高了20-30%。现已在国内外多个蛋白质组学研究实验室得到应用并获得好评(Mol. Cell. Proteomics, 2011, 10.1074/mcp.M110.006452),2013年应Nature Protocol的邀请,与荷兰国家蛋白质组学研究中心的Heck教授合作,发表了Ti4+-IMAC的制备及其在蛋白质磷酸化分析中应用的论文(Nat. Protoc.,2013, 8, 3, 461-480)。经过不断优化,现已发展出用于快速、高效溶液富集方法的单分散亲水性高分子微球和用于固相萃取微柱的高分子聚合物大微球两种新型Ti4+-IMAC磷酸肽富集材料,可以实现快速、高效、低成本的磷酸肽富集(Nature Chemical Biology, 2016, 12, 959-968; J. Chromatogr. A, 2017, 1498, 22–28)。此外,除了可以实现复杂生物样品中磷酸肽的高特异性富集,我组科研人员还发现Ti4+-IMAC也可以对糖肽进行高效富集(Anal. Chem. 2019, 91, 18, 11589–11597;Anal. Chem. 2021, 93, 21, 7579–7587;Anal. Chem. 2021, 93, 24, 8568–8576)。(文/图 胡颂华,刘晓艳)