早期胃癌无明显症状且存在较长的潜伏期,具有诊断迟、转移快和治疗效率低等问题。临床上现有的胃癌血清标志物有CEA、CA125、CA72-4和CA19-9等,但它们对胃癌诊断的特异性和敏感度较差,难以用于胃癌的早期诊断。最近,我组联合空军军医大学聂勇战教授等人开发了一种用于位点特异性糖型分析的高稳健蛋白质组分析平台,对278例临床样本进行N-糖基化蛋白质组的规模化分析,筛选并验证了可诊断胃癌尤其是早期胃癌的新型蛋白质糖基化类生物标志物—位点特异性糖型。相关成果以“Robust Glycoproteomics Platform Reveals a Tetra-Antennary Site-Specific Glycan Capping with Sialyl-Lewis Antigen for Early Detection of Gastric Cancer”为题,发表在《先进科学》(Advanced Science)上。
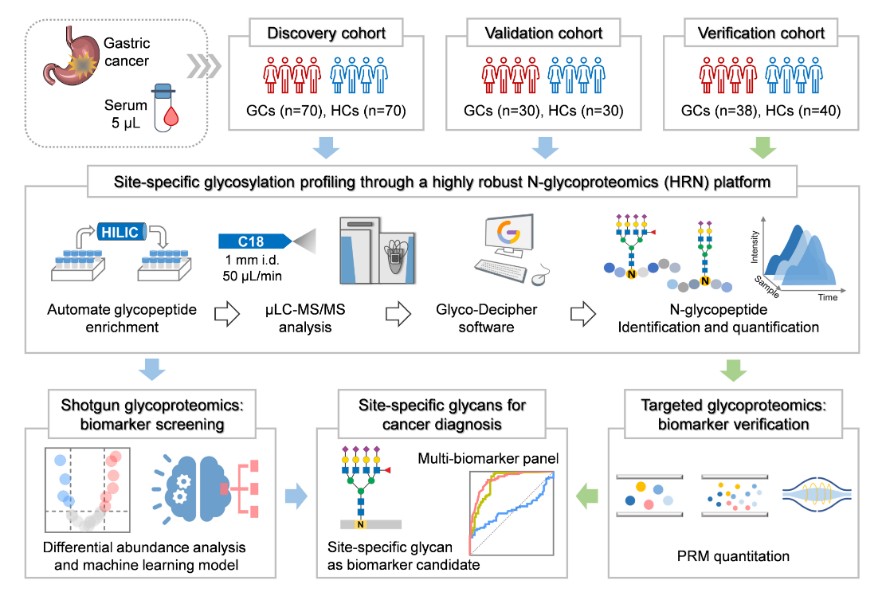
图1:通过高稳健的N-糖蛋白质组学平台发现血清位点特异性糖型疾病标志物的工作流程。
位点特异性糖型是指发生在特定蛋白质特定位点的糖型。现有在临床上使用的肿瘤标志物基本都是糖基化蛋白质,在使用中要么只检测蛋白质的浓度,要么只检测某类糖型的浓度(如 CA199 就是一类糖抗原),目前几乎没有基于特定位点糖型的疾病标志物。鉴于蛋白质的糖基化修饰与肿瘤的发生密切相关,在组学层次进行位点特异性糖型的分析有望发现新型疾病标志物,提高基于蛋白质糖基化的精准医学研究水平,但其分析仍然面临严峻挑战。为了解决这一问题,团队采用自动化方法富集生物样本中的N-完整糖肽,采用微流LC-MS/MS系统检测N-完整糖肽,最后采用自主开发的Glyco-Decipher软件鉴定并定量位点特异性糖型,从而建立了一套高稳健的糖蛋白质组分析平台(图1)。使用该平台分析了200多个样品,富集特异性保持在88.1%-91.7%,在10个批内/批间的质量控制样本中,不同考察层次鉴定数目的相对标准偏差均低于7%,且定量N-完整糖肽的Pearson相关系数平均值为0.909。在长时间分析大队列样本后,每个质量控制样本依然能稳定地鉴定到平均1900条N-完整糖肽。因此,该平台具有高灵敏、高稳健的N-完整糖肽鉴定能力,为 N-糖基化位点特异性糖型的规模化分析提供了一个有力的分析工具。
将该平台应用于筛选新型位点特异性糖型胃癌标志物。团队首先采用发现蛋白质组学策略,在发现和验证队列分别进行N-糖蛋白质组分析,共鉴定到来自971种糖蛋白上的21711种位点特异性糖型。通过差异分析和构建机器学习随机森林模型,筛选到四个位点特异性糖型作为候选生物标志物。它们对胃癌患者均展现了优异的诊断性能,尤其是联合诊断早期胃癌的AUC值大于0.91,而传统胃癌血清标志物癌胚抗原(CEA)的诊断AUC值则小于 0.67。随后,团队利用该系统并采用靶向糖蛋白质组学分析策略,在单独的靶向验证队列中,验证了这四个位点特异性糖型对胃癌和早期胃癌优异的诊断性能。
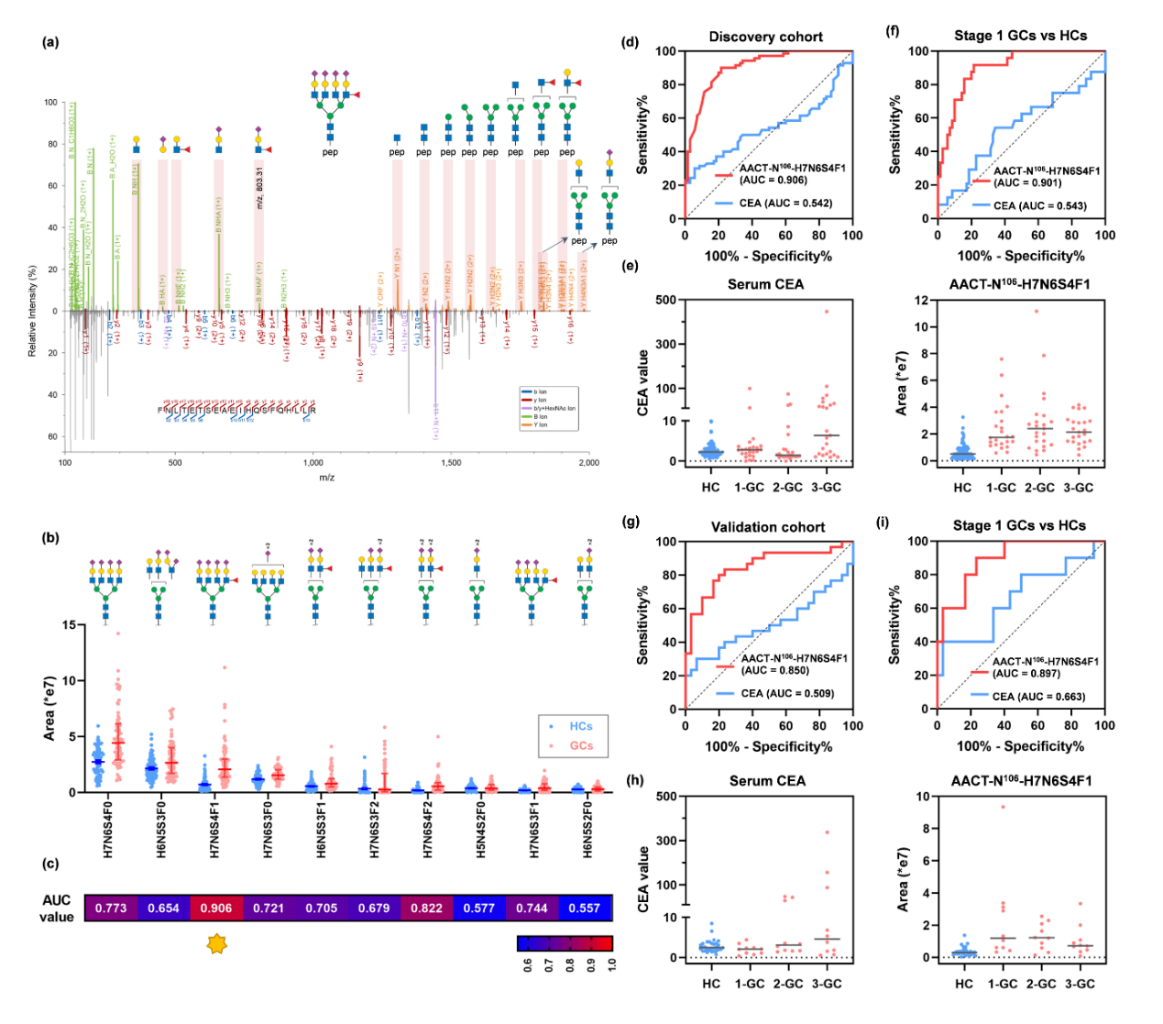
图2:AACT-N106-H7N6S4F1作为胃癌疾病诊断的特征。(a) FNLTETSEAEIHQSFQHLLR- H7N6S4F1糖肽(对应于AACT-N106-H7N6S4F1位点特异性糖型)的MS2谱图。发现队列中AACT-N106位点上的前10位高丰度聚糖的表达分布(b)和胃癌诊断的AUC值(c)。在发现队列中,诊断胃癌(d)和早期胃癌(f)的ROC曲线,以及血清CEA和AACT-N106-H7N6S4F1的丰度分布(e)。在验证队列中,诊断胃癌(g)和早期胃癌(i)的ROC曲线,以及血清CEA和AACT-N106-H7N6S4F1的丰度分布(h)。
在分析结果中,发现带有SLe抗原的四天线糖链结构位点特异性糖型(AACT-N106-H7N6S4F1)对胃癌的诊断性能远优于同位点上的其他糖型。借助 该分析平台的高灵敏度鉴定,AACT-N106位点上共检测到 159 种 N-糖型,展现了 AACT 蛋白糖基化的高度异质性。接着选择 AACT-N106 位点上相对丰度前10的位点特异性糖型,考察它们在发现队列中的诊断性能(图 2b)。与 AACT-N106 位点其他 N-糖链相比,H7N6S4F1 表现出最佳的诊断性能(图 2c),其 AUC 值为 0.906,说明位点特异性糖型作为新型生物标志物的潜力。该位点特异性糖型对胃癌的早期诊断能力也显著优于CEA(图 2d-h)。
叶明亮团队长期致力于位点特异性糖型分析方法的发展,在糖肽的分离和富集方面发展了O-GlcNAc糖肽的可逆酶促化学标记策略(Angew. Chem. Int. Ed.,2022)、自动化的N-完整糖肽富集方法(Anal. Chem.,2021)、同时富集和鉴定N-和O-完整糖肽的分析方法(Anal. Chem.,2023);在糖肽的谱图解析软件方面,分别发展了O-糖肽的检索策略O-search(Anal. Chem.,2019;Anal. Chem.,2023;Bioinformatics,2022)和N-糖肽质谱谱图的解析软件Glyco-Decipher(Nat. Commun.,2022)。目前,Glyco-Decipher软件可以从github.com网站下载,由于其解析灵敏度高、界面友好,已被很多课题组和生物公司采用(文/图 刘璐瑶、刘蕾)
文章链接:https://doi.org/10.1002/advs.202306955