近日,我组PELSA团队自主研发的AutoPELSA自动化处理平台正式上线,搭配东北地区首套Astral高分辨质谱系统,将配体靶标鉴定效率提升了整整一个数量级,持续领跑配体靶标鉴定赛道!
PELSA(以肽段为中心的蛋白质局部稳定性分析技术)是我们团队独立开发的核心技术,2025年登上《Nature Methods》,是目前全球领先的无需配体化学修饰的靶标鉴定技术:
² 相比同类LiP-MS技术,靶标鉴定灵敏度提升10倍;
² 相比传统热蛋白质组技术(TPP),灵敏度提升2.4倍;
² 可同时实现靶蛋白鉴定、结合区域定位、亲和力测定三大核心功能;
² 无需对配体进行任何化学修饰,最大程度还原真实结合状态。
PELSA技术问世以来,我们已经为几十家高校、科研院所和药企提供了靶标筛选服务,覆盖药物、中药单体、天然产物、代谢物、环境污染物等多个研究领域。但我们也注意到,传统手动PELSA流程操作繁琐、通量有限,难以满足大规模筛选需求。经过团队近两年的技术攻关,推出了全自动化的AutoPELSA处理平台,彻底解决了手工操作的痛点!
AutoPELSA三大核心升级,重新定义高通量靶标鉴定
1. 效率跃升:从"天"到"小时"的跨越
AutoPELSA将整个实验流程(限制性酶切、胰酶去除、肽段脱盐)全部整合到自动化移液工作站中(图1),兼容96孔板操作:
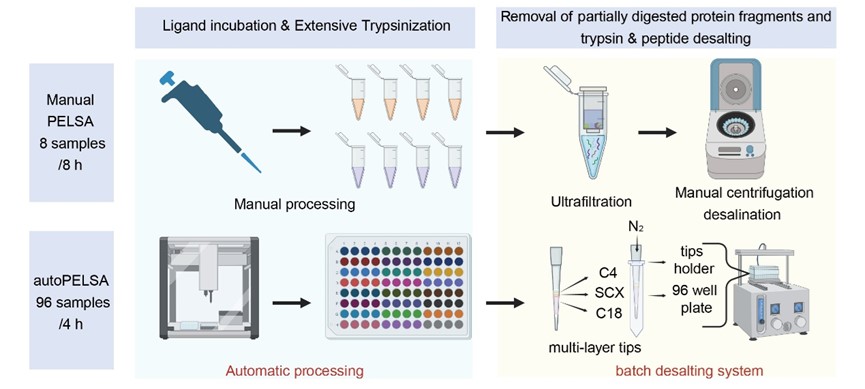
图1. AutoPELSA的操作流程
· 样品处理速度:仅需4小时即可完成96个样品的全流程处理;
· 整体实验周期:搭配全新Astral质谱系统,单日可完成约60个样品的数据采集,相当于每天可以完成至少7个配体的单剂量点实验,相比传统手动方案,整体通量提升了10倍以上!
2、稳定性与灵敏度双重突破
自动化不仅带来了速度,更带来了实验质量的全面提升:
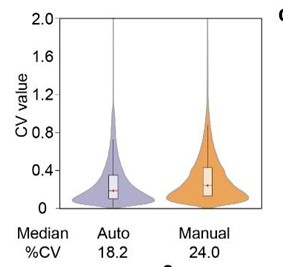
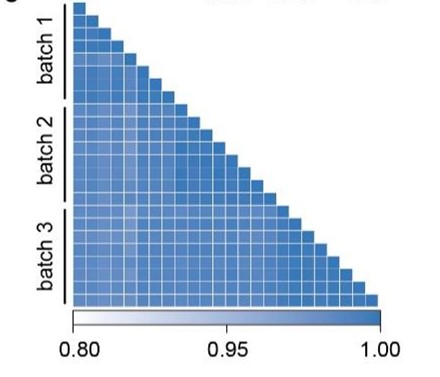
图2. 左:AutoPELSA与手动操作的对比;右:AutoPELSA三个批次的皮尔森相关系数
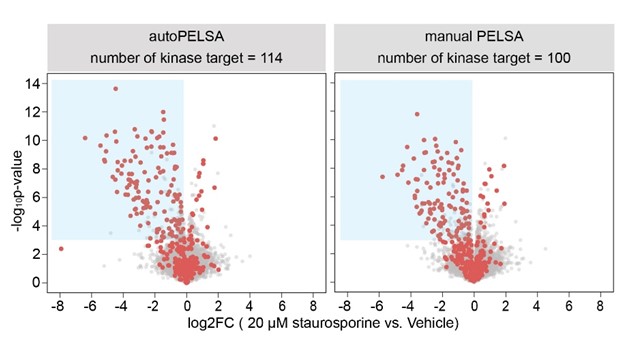
图3. AutoPELSA与手动鉴定星孢菌素靶标的火山图对比
· 定量准确性:自动化操作下肽段定量变异系数(CV%)仅为18.2%,显著优于手动操作的24.0%(图2左);
· 批次重复性:三个独立批次样品的肽段定量皮尔森相关系数均≥0.94,实验结果高度稳定(图2右);
· 检测深度:通量提升的同时,质谱检测深度反而提高了近30%,低丰度靶标 检出能力大幅增强;在经典激酶抑制剂星孢菌素的靶标鉴定测试中,同等条件下AutoPELSA鉴定到114个激酶靶标,比手动方案多检出14个,靶标覆盖度显著提升(图3)
3、技术创新:多层固相萃取柱设计
我们自主设计了C4-SCX-C18三层固相萃取柱,开创性地将胰酶去除与肽段脱盐整合为单一步骤:
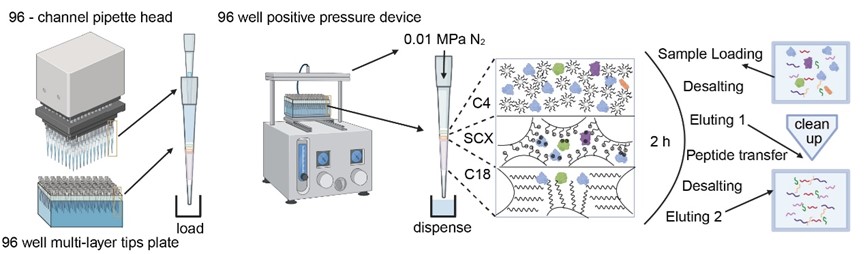
图4.多层固相萃取柱的设计和操作流程
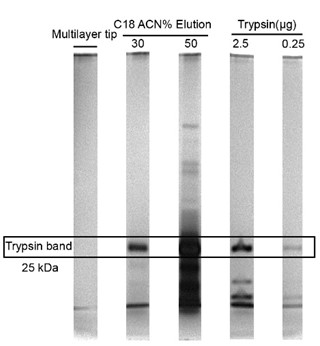
图5. 不同填料处理PELSA酶切后样品中胰酶的剩余量测定
· 搭配正压装置,可实现96个样品同步处理,真正实现高通量(图4);
· 相比传统单层C18填料,胰酶去除更彻底,杂质干扰更少(图5)。
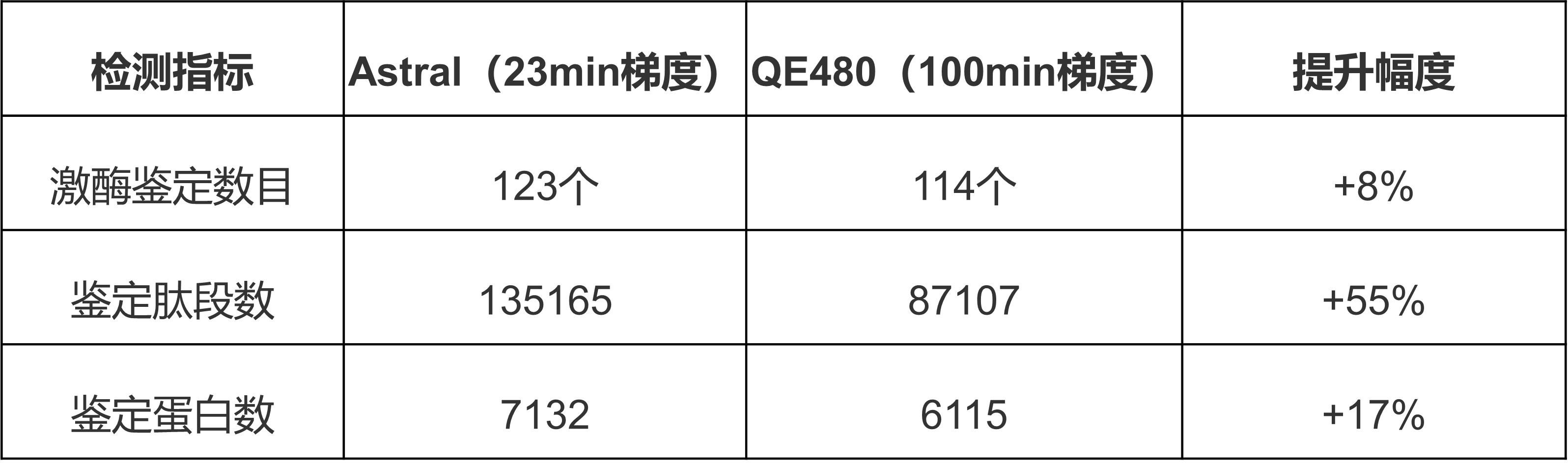
4、Astral质谱加持:东北首套,性能再攀高峰
除了自动化平台,我们还全新引入了东北地区首套Astral高分辨质谱系统,将检测能力推向了新高度。仅仅23分钟的短梯度,就能超过传统质谱100分钟长梯度的鉴定效果,大幅缩短了数据采集周期,特别适合大规模样品筛选。
5、AutoPELSA实际应用场景展示
场景1:低亲和力代谢物靶标鉴定
针对低亲和力配体检测这一行业难题,我们用代谢物α-酮戊二酸(α-KG)进行了测试:
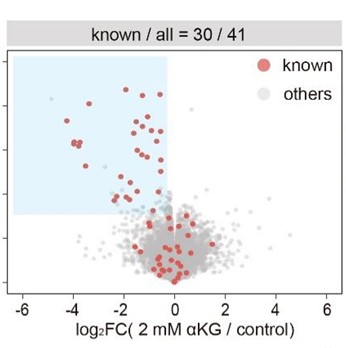
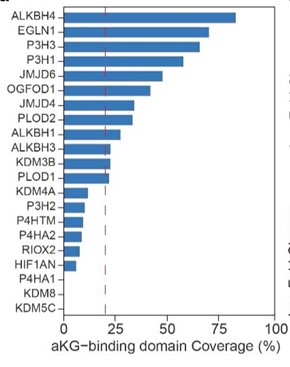
图6. 左:2 mM α-酮戊二酸的靶标鉴定效果;右:在21个已知靶点(-log10(pvalue) > 3)的注释αKG结合域内的肽段覆盖情况
在2mM α-KG条件下,AutoPELSA成功鉴定出41个显著被配体稳定的蛋白,其中30个为已报道靶标(图6左),并且可以精准定位到配体结合区域(图6右),对于研究代谢物-蛋白互作、表观遗传调控等方向有极大价值。
场景2:混合配体高通量亲和力测定
传统亲和力测定需要对每个配体单独做浓度梯度,实验成本高、周期长。我们开发了混合配体错位浓度梯度策略,单次实验即可同时测定4种不同配体的全蛋白质组水平亲和力(图7a)
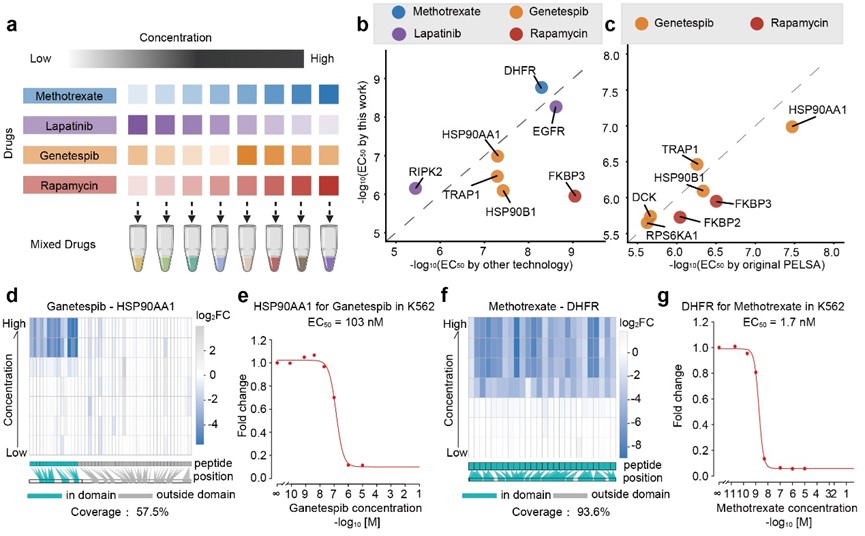
图7. 混合配体的靶蛋白亲和力测定
· 获得的EC50值与酶活实验、荧光偏振等正交方法结果高度一致(图7b);
· 与手动PELSA单配体测定结果完全吻合(图7c);
· 配体结合信号仅出现在已注释的结合结构域,特异性极强(图7d-g);
AutoPELSA技术平台特别适合新药研发早期的化合物靶点筛选,可大幅降低筛选成本、缩短研发周期。相关成果以“AutoPELSA: an automated sample preparation system for proteome-wide identification of target proteins of diverse ligands”为题,发表在预印本平台biorxiv上。(文/图 薛连基、张晓磊)
文章链接:https://www.biorxiv.org/content/10.64898/2026.01.08.697612v1